درمان سرطان با مهار مهارکنندهها!
بدست پزشكان گيل • 4 اکتبر 2018 • دسته: تیتر اول٬ ویژه نوبل ۲۰۱۸نوبل پزشکی یا فیزیولوژی ۲۰۱۸
ترجمه: دکتر هدیه حجفروش
سرطان سالانه جان میلیونها انسان را میگیرد و یکی از بزرگترین چالشهای سلامت آدمی است. برندگان جایزه نوبل امسال، با تحریک توانایی ذاتی دستگاه ایمنی بدن برای حمله به سلولهای سرطانی، اصولی کاملاً نوین در درمان سرطان بنا نهادند.
جیمز پی آلیسون بر یک پروتئین شناختهشده که بهعنوان مهارکننده دستگاه ایمنی بدن کار میکند مطالعه کرد. او نشان داد که برداشتن این مهار و بهدنبال آن رها کردن دستگاه ایمنی، میتواند سبب حمله به تومورهای سرطانی شود. وی سپس این مفهوم را به رویکرد جدیدی برای درمان بیماران تبدیل کرد.
به موازات تلاشهای آلیسون، تاسوکو هونجو پروتئینی در سلولهای ایمنی کشف کرد که پس از کشف دقیق جزییات کارکرد آن، سرانجام آشکار شد که این پروتئین هم بهعنوان یک عامل مهاری اما با مکانیسم متفاوت کار میکند. او ثابت کرد که درمانهای حاصل از این کشف میتواند بهطور بسیار قابلتوجهی در مبارزه با سرطان موثر باشد.
آلیسون و هونجو نشان دادند چگونه راهبردهای متفاوت برای جلوگیری از این مهارهای دستگاه ایمنی، میتواند در درمان سرطان مورد استفاده قرار گیرد. کشفهای اولیه این دو دانشمند برجسته به نقطه عطفی در مبارزه علیه سرطان تبدیل شد.
آیا دستگاه ایمنی ما میتواند برای درمان سرطان بهکار رود؟
سرطان شامل بیماریهای مختلفی است که مشخصه همه آنها، رشد غیرقابل کنترل سلولهای غیرطبیعی با قابلیت تهاجم به بافتها و اندامهای سالم است. چندین رویکرد درمانی برای درمان سرطان در دسترس است؛ از جمله جراحی، پرتودرمانی (رادیوتراپی) و برخی روشهای دیگر که به برخی از آنها پیشتر جایزه نوبل اهدا شده است: هورموندرمانی برای سرطان پروستات (هاگینز، ۱۹۶۶)، شیمیدرمانی (الیون و هیتچینز، ۱۹۸۸) و پیوند مغز استخوان برای درمان لوسمی (تامس، ۱۹۹۰). با اینهمه، درمان سرطانهای پیشرفته همچنان بسیار سخت است و به راهبردهای درمانی جدیدتری نیاز دارد.
در اواخر قرن نوزدهم و شروع قرن بیستم این مفهوم آشکار شد که فعالسازی دستگاه ایمنی میتواند راهکاری برای حمله به سلولهای سرطانی باشد. بدینمنظور تلاشهای متعددی شکل گرفت تا بیماران را با باکتریها آلوده و دستگاه دفاعی بدن را فعال کنند. این تلاشها بهنسبت اثر کمی داشت البته نوع دیگری از این راهکار، امروزه در درمان سرطان مثانه مورد استفاده قرار میگیرد. دانشمندان بسیاری شروع به انجام پژوهشهای بنیادین زیادی کردند تا پرده از مکانیسمهای اساسی تنظیمکننده دستگاه ایمنی بردارند و نیز نشان دهند که سلولهای ایمنی چطور سلولهای سرطانی را شناسایی میکنند. با وجود پیشرفتهای قابلتوجه علمی، ثابت شد تلاش برای ابداع راهکارهای جدید قابل تعمیم، در برابر سرطان بسیار دشوار است.
تسریعکنندهها و مهارهای دستگاه ایمنی ما
ویژگی اساسی دستگاه ایمنی ما توانایی شناسایی «خودی» از «غیرخودی» است، بنابراین میتواند به باکتری، ویروس و سایر عوامل خطرزای مهاجم حمله و آنان را پاکسازی کند. لنفوسیت T که نوعی گلبول سفید است، در این دفاع نقشی کلیدی دارد. این لنفوسیتها گیرندههایی دارند که به عواملی که بهعنوان غیرخودی شناخته شدهاند، متصل میشوند و همین تعامل، راهانداز دستگاه ایمنی برای شروع دفاع است. اما به پروتئینهای دیگری که بهعنوان تسریعکنندههای سلول T عمل میکنند، نیز نیاز است تا شاهد یک پاسخ همهجانبه دستگاه ایمنی باشیم. دانشمندان بسیاری در این پژوهشهای بنیادین بسیار مهم سهم داشتند و پروتئینهای دیگری را که بهعنوان مانع روی سلول T، در مهار دستگاه ایمنی نقش دارند، شناسایی کردند. این تعادل پیچیده بین تسریعکنندهها و عوامل مهاری برای کنترل دقیق ضروری است و تضمین میکند که دستگاه ایمنی در حالی که به اندازه کافی درگیر حمله به میکروارگانیسمهای خارجی میشود، از فعالیت بیش از حد که منجر به تخریب خودایمن سلولها و بافتهای سالم بدن میشود، اجتناب کند.
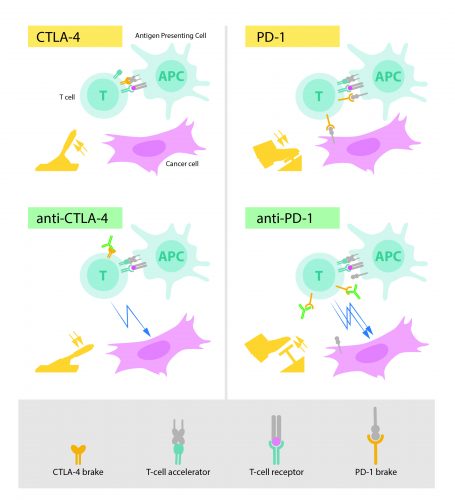
چپ بالا: برای فعالسازی سلول T، لازم است که گیرنده این سلول به سازههایی در سلولهای ایمنی دیگری که بهعنوان «غیرخودی» شناخته میشوند، متصل شود. علاوه بر این، برای فعال شدن سلول T به پروتئینی نیز نیاز است که بهعنوان تسریعکننده عمل میکند. CTLA-4 بهعنوان یک عامل مهاری روی سلولT عمل میکند و مانع از عمل تسریعکنندهها میشود.
چپ پایین: آنتیبادیها (سبز) علیه CTLA-4، عملکرد مهاری آن را که مانع از فعالسازی سلول T و حمله به سلولهای سرطانی است، مسدود میکند.
راست بالا: PD-1 یکی دیگر از عوامل مهارکننده سلولT است که مانع از فعال شدن این سلول میشود.
راست پایین: پادتنهای علیه PD-1مانع از مهار فعالیت سلول T و سبب حمله موثر به سلولهای سرطانی میشود.
اصلی جدید برای ایمنیدرمانی
جیمز پی آلیسون در دهه ۱۹۹۰ در آزمایشگاه خود در برکلی در دانشگاه کالیفرنیا روی گیرنده پروتئینی CTLA-4 سلولهای T مطالعه میکرد. او یکی از چند دانشمندی بود که مشاهده کرده بودند گیرنده پروتئینی CTLA-4 همانند یک مهار روی سلول T عمل میکند. سایر تیمهای پژوهشی از این یافته بهعنوان هدفی برای درمان بیماریهای خودایمنی استفاده کردند. با اینهمه آلیسون عقیده کاملاً متفاوتی داشت. او یک پادتن (آنتیبادی) ساخت که میتوانست به این گیرنده متصل شود و عملکرد آن را مهار کند. سپس شروع به تحقیق در اینباره کرد که آیا مسدود کردن این گیرنده میتواند مهار سلول T را رها کند و دستگاه ایمنی را برای حمله به سلولهای سرطانی فعال سازد؟ آلیسون و همکارانش اولین آزمایشهای خود را در اواخر سال ۱۹۹۴ انجام دادند و با توجه به هیجانی که داشتند این آزمایش را بلافاصله در تعطیلات کریسمس هم تکرار کردند. نتایج آزمایشها دیدنی بود؛ موشهای مبتلا به سرطان با درمان با پادتنهایی که ترمزها را مهار و فعالیت ضدسرطانی سلولهای T را آزاد میکرد، درمان شدند. با وجود ابراز علاقه ناچیز صنایع دارویی، آلیسون تلاش بسیار خود را برای توسعه راهکارهای درمانی برای درمان انسانها ادامه داد. بهزودی نتایج امیدوارکنندهای از گروههای مختلف پدیدار شد و در سال ۲۰۱۰ یک مطالعه بالینی مهم، اثرات قابلتوجهی در بیماران مبتلا به ملانوم پیشرفته نشان داد. در چندین بیمار علایم سرطان باقیمانده ناپدید شد. چنین نتایجی پیش از این هرگز در این گروه از بیماران مشاهده نشده بود.
کشف PD-1 و اهمیت آن در درمان سرطان
در سال ۱۹۹۲، چند سال پیش از کشف آلیسون، تاساکو هونجو PD-1 را کشف کرد؛ پروتئین دیگری که در سطح سلول T وجود دارد. هونجو در تلاش برای رمزگشایی نقش این پروتئین، سالها با دقت و وسواس فراوان مجموعهای از آزمایشهای دقیق را در آزمایشگاه خود در دانشگاه کیوتو انجام داد. نتایج نشان داد که PD-1 همانند CTLA-4 بهعنوان مهارکننده سلول T اما با مکانیسم دیگری کار میکند. آزمایشهایی که روی حیوانات انجام شد، همانند کارهای هونجو و سایر گروهها، نشان داد که مسدود کردن PD-1 میتواند راهکاری امیدبخش در جنگ با سرطان باشد. این یافته راه را برای استفاده از PD-1 بهعنوان یک هدف در درمان بیماران هموار کرد. توسعههای بالینی بعدی و یک مطالعه کلیدی در سال ۲۰۱۲ اثربخشی واضح آن را در درمان بیماران با انواع مختلف سرطان نشان داد. نتایج بسیار تاثیرگذار بود و منجر به پسرفت (remission) طولانیمدت و امکان درمان در چندین بیمار با سرطانهای متاستاتیک شد؛ شرایطی که قبلاً لزوماً غیرقابل درمان در نظر گرفته میشد.
ایمنیدرمانی سرطان امروز و در آینده
پس از مطالعات اولیه که تاثیر مسدودسازی CTLA-4 و PD-1 را نشان داد، پیشرفتهای بالینی بسیار چشمگیر بود. امروزه میدانیم درمانی که اغلب به نام«درمان ایست بازرسی دستگاه ایمنی» (immune checkpoint therapy) از آن نام میبرند ، بهطور اساسی سرنوشت گروههای خاصی از بیماران مبتلا به سرطانهای پیشرفته را تغییر داده است. مشابه سایر درمانهای سرطان، عوارضی هم دیده میشود که ممکن است جدی و حتی تهدیدکننده زندگی باشد. این عوارض معمولاً ناشی از پاسخ بیش از حد دستگاه ایمنی است که میتواند سبب واکنشهای خودایمن شود اما معمولاً قابل کنترل است. تحقیقات دقیق با تمرکز بر روشنسازی مکانیسم عمل و با هدف بهبود درمان و کاهش عوارض ادامه دارد.
از دو راهکار درمانی، ثابت شده که درمان ایست بازرسی دستگاه ایمنی علیه PD-1 موثرتر است و نتایج مثبت بیشتری در درمان چندین نوع سرطان از جمله سرطان ریه، سرطان کلیه، لنفوم و ملانوم مشاهده شده است. مطالعات بالینی جدید نشان میدهد که درمان ترکیبی با هدف گرفتن هر دو گیرنده CTLA-4 و PD-1 چنانچه در بیماران مبتلا به ملانوم نشان داده شده، موثرتر هم هست. بنابراین آلیسون و هونجو الهامبخش تلاشهایی شدند که راهکارهای مختلف را برای رهاسازی مهارکنندههای دستگاه ایمنی، با هدف پاکسازی سلولهای سرطانی به روشهای موثرتر، ترکیب میکند. تعداد زیادی از این روشهای مطالعاتی در حال حاضر علیه انواع مختلف سرطان در حال انجام است و پروتئینهای مهاری متعددی هم بهعنوان هدف در دست آزمایش و بررسی هستند.
بیش از صد سال است دانشمندان در تلاشاند تا دستگاه ایمنی را در مبارزه علیه سرطان بهکار گیرند. تا پیش از کشف اولیه این دو دانشمند نخبه، پیشرفتهای بالینی نسبتاً اندک بود. این روش درمانی انقلابی در درمان سرطان ایجاد کرد و راهکارهای کنترل سرطان را از پایه دگرگون ساخت.
From: nobelprize.org
دکتر هدیه حجفروش
پزشک عمومی
Email: dr.hajf@gmail.com

۱ اکتبر ۲۰۱۸
جایزه نوبل فیزیولوژی یا پزشکی سال ۲۰۱۸ مشترکاً تقدیم شد به:
جیمز پی آلیسون (James P. Allison) و تاسوکو هونجو (Tasuku Honjo)
بهپاس کشف درمان سرطان با مهار تنظیم منفی دستگاه ایمنی بدن.
 جیمز پی آلیسون
جیمز پی آلیسون
متولد ۷ آگوست ۱۹۴۸، شهر آلیس، ایالت تگزاس، آمریکا
محل اشتغال در زمان اهدای جایزه: مرکز سرطان دکتر آندرسون در دانشگاه تگزاس، شهر هیوستون، ایالت تگزاس، آمریکا؛ موسسه ایمونولوژی سرطان پارکر، شهر سانفرانسیسکو، ایالت کالیفرنیا، آمریکا
 تاسوکو هونجو
تاسوکو هونجو
متولد ۲۲ ژانویه ۱۹۴۲، کیوتو، ژاپن
محل اشتغال در زمان اهدای جایزه: دانشگاه کیوتو، کیوتو، ژاپن

پزشكان گيل
فرستادن نامه به این نویسنده | همهی نوشتههای پزشكان گيل
